En el món desenvolupat, on la majoria de les malalties infeccioses, gran problema de la resta del planeta (encara que això sembla que ens la rebufi...), estan sota control, els nostres esforços investigadors es dirigeixen vers altres problemes que emergeixen en absència d'aquestes. Un dels focus més importants se situa en el camp dels trasplantaments d'òrgans (un dels hàbits més comuns dels “civilitzats” és intoxicar els propis òrgans amb alcohol, tabac i greix 100% pur amb sal per sobre i després posi’m sacarina, que m’he passat...). Aconseguirem fer bastides per al cor? De Flickr
Mentre que en el cas d’altres òrgans, com ara el fetge, les capacitats de regeneració del propi teixit donen l’esperança d’utilitzar cèl•lules sanes del propi òrgan del pacient per tal de regenerar les parts danyades, en el cas del cor, aquesta possibilitat queda pràcticament descartada: el cor té una pèssima capacitat autoregenerativa (al menys físicament parlant, perquè a qui no li han trencat el cor alguna vegada, i encara està per aquí pul•lulant? D’acord, acudit dolent...).
Però vet aquí que, entre totes les alternatives possibles emprades fins ara, amb millors o pitjors resultats, n’apareix a l’horitzó una de nova, que es publica avui a Nature Medicine, i que alguns han batejat com a “Cor fantasma”... En què consisteix?
Per començar, deixem clar que la cosa ara com ara s’ha fet amb rates i ha donat resultats esperançadors, però no operatius. Ja sabeu el què això significa? No? Jo us ho explico: que igual no s’aconsegueixen resultats millors que aquests en les pròpies rates, que igual no s’aconsegueixen resultats semblants en humans, que igual vés a saber què pot arribar a passar en el llarguíssim camí que separa una experiència in vitro d’una in vivo. Dit això, un cop posats els peus a terra, vegem que han fet Doris Taylor i els seus col•laboradors de la Universitat de Minnesota.
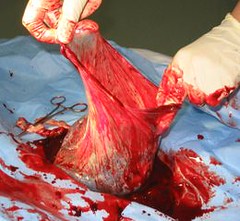
Partint del cor d’una rata, n’han eliminat totes les cèl•lules mitjançant detergents (no penseu en l’ajax pino o el dixan, encara que la cosa té uns efectes similars...) i se n’ha deixat només l’estructura bàsica (o sigui, la bastida sobre la qual hi havia les cèl•lules) formada per fibres i altres substàncies no cel•lulars. Això és el que alguns han anomenat un "cor fantasma". Sobre aquesta bastida, o "cor fantasma" es van injectar cèl•lules que provenien del cor d’una rata acabada de néixer i que, tot i no ser cèl•lules mare, si que tenen la capacitat de diversificar-se en tots els tipus de cèl•lula que trobem en el cor de l’adult.
Doncs bé, els resultat obtingut ha estat que, en l’estructura de la bastida de la rata adulta, les cèl•lules introduïdes van formar una estructura de teixit que, al cap d’un temps va començar a bategar i presentar el comportament d’un cor normal. No obstant, i com us dèiem abans, els resultats de moment són només esperançadors, ja que si bé el teixit bategava, el batec era mínim respecte el que requeriria un cor funcional normal (en aquest sentit es parla de la necessitat de més temps i/o d’introducció de més quantitat de cèl•lules).
En el cas que aquesta tècnica es perfeccionés en el seu model per a rates, es podria començar a plantejar la possibilitat de seguir el mateix camí en humans, introduint cèl·lules mare en un cor fantasma adequat per a humans. Els primers candidats per fer de bastida cardíaca humana ja es comencen a apuntar: cors obtinguts de cadàvers humans, bastides artificials, o fins i tot, la bastida del cor de l’animal amb el sistema circulatori més semblant al dels humans (i no és cap acudit): EL PORC.
15/1/08
El "Cor fantasma" i el futur dels trasplantaments
Publicat per
Quim ADSADN
a les
8:41
2
comentaris
![]()
Etiquetes: Actualitat, Cèl·lules mare, Fisiologia
25/11/07
Aquí no es llença res
Això era un home tan lleig, tan lleig, tan lleig, que quan va néixer la seva mare no sabia si quedar-se amb ell o amb la placenta.
Si aquesta dona hagués llegit el review presentat per Toda i col·laboradors, potser no s'hauria quedat amb la placenta, però sí amb el sac amniòtic.
L'amnios és la membrana interna del sac amniòtic, conté el famós líquid amniòtic, és d'origen fetal i es compon d'una sèrie de capes sense nervis, músculs o vasos sanguinis; normalment acaba en les escombraries després del part. Però l'article esmentat abans ofereix un resum de les dades experimentals més rellevants sobre l'ús de la membrana amniòtica i les seves cèl·lules derivades en el terreny de la medicina regenerativa.
La medicina regenerativa és un nou camp basat en l'ús de cèl·lules mare per a generar substituts biològics o millorar les funcions dels teixits, i sobretot com a alternativa al transplantament d'òrgans.
Les cèl·lules derivades de l'amnios tenen una habilitat de diferenciació multipotent i han atret l'atenció com a font de cèl·lules mare, car poden diferenciar-se en qualsevol de les tres capes germinals que donen lloc als teixits de l'embrió: endoderm (fetge, pàncrees...), mesoderm (cor, músculs, esquelet...), i ectoderm (cèl·lules nervioses, pell...); són poc inmunogèniques, tenen funcions antiinflamatòries i no requereixen sacrificar embrions humans, encara que després del que s'ha llegit en la (pèssima) premsa espanyola aquesta última setmana semblés que fins ara no podien aconseguir-se cèl·lules mare sense destruir embrions, el cert és que des de fa temps se sap que existeixen altres fonts de matèria primera per a tenir cèl·lules mare (si bé no tenen exactament les mateixes característiques que les cèl·lules mare embrionàries, és clar; aquest és l'autèntic secret de la notícia presentada recentment).
Perquè les cèl·lules mare puguin fer-se servir com a substitutes d'un teixit calen tres coses: que conservin la seva capacitat d'autoregeneració, que proliferin ràpidament i que puguin diferenciar-se en altres tipus cel·lulars; a més cal proveir-les d'algun tipus de superfície que serveixi de bastida per a la seva proliferació i proporcionar-les factors de creixement i de diferenciació.
Fins ara les cèl·lules mare preferides eren les embrionàries i les obtingudes a partir de teixits adults, però ambdues presenten uns problemets que han estat poc airejats a la premsa generalista, que prefereixen centrar-se en els missatges sensacionalistes de l'estil "demà dijous guarirem el càncer".
Per exemple, les cèl·lules mare d'adult són difícils d'aïllar i fer créixer en el laboratori en nombre suficient com per a transplantar-les a gran escala. Les cèl·lules mare embrionàries, en canvi, creixen a corre-cuita, fins el punt que cal controlar el seu creixement perquè no formin tumoracions. A més requereixen el sacrifici d'embrions humans (almenys fins ara), amb les implicacions ètiques que això comporta.
Afortunadament es va descobrir que les cèl·lules derivades de l'amnios també podien diferenciar-se en altres teixits i tenien molts avantatges. Fins fa poc la membrana amniòtica es feia servir en lesions de cremades, oftalmologia i altres usos mèdics. Les seves propietats antiinflamatòries fan que els transplantaments de membrana amniòtica no deixin cicatriu. També tenen propietats antiangiogèniques, antibacterianes, i generalment no produeixen forts rebutjos inmunològics ni tumoracions. Per a aïllar aquestes cèl·lules n'hi ha prou amb raspar-les mecànicament del còrion d'una placenta i preparar-les per al seu cultiu.
S'ha comprovat que poden diferenciar-se en hepatocits,per exemple, i s'està investigant el seu ús com a font de matèria primera de cèl·lules mare no hepàtiques per al transplantament de fetge (les cèl·lules obtingudes a partir de cordó umbilical i medul·la òssia, sembla ser que donen alguns problemets).
El mateix per a cardiomiocits: les cèl·lules mare d'altres procedències aplicades al transplantament de cor donen problemes de rebuig inmunològic, tumurogènesi, nombre de cèl·lules requerides i problemes ètics; les cèl·lules mare de l'amnios podrien superar aquests inconvenients. I s'investiga en aplicar-les en el terreny de la regeneració neurològica, auditiva, pancreàtica o del cartílag.
A més, aquest mateix grup d'investigació està desenvolupant noves superfícies de cultiu cel·lular, cobertes per un polímer basat en proteïnes que permet el cultiu en capes d'aquestes cèl·lules, així com en millors maneres de conservació de l'amnios, més pràctiques que l'amnios fresc congelat que es venia fent servir.
Així que l'amnios no només constitueix una font interessant de cèl·lules mare no embrionàries sinó que les cèl·lules que ho componen permeten crear materials que obren un nou camp en l'enginyeria tisular. Al final resultarà que no cal llençar gens, que tot es recicla.
Publicat per
Elena Garrido
a les
10:55
0
comentaris
![]()
Etiquetes: Actualitat, Cèl·lules mare, Medicina